
Enkla tekniska experiment är mycket användbara att göra med barn, det här är att spendera tid tillsammans, införa färdigheter och förståelse för små designers, grunderna, att bröden, som i den berömda tecknen, inte växer på träd.
Den här gången beslutade vi att göra den enklaste kemiska strömkällan och försöka tillämpa den för allt praktiskt. På tal om den praktiska tillämpningen är det värt att erinra om att för bara några generationer sedan erbjöds radioamatörer för att leverera sina batteriradiomottagare och förstärkare att tillverka flera typer av galvaniska celler eller batterier för oberoende produktion. Dessa är elementen i Leklanshe och Popov [1] s. 9 ... 18, eller ett blypotash eller gasbatteri [1], s. 22 ... 28. Flera, relativt högströmselement var anslutna till ett glödande batteri (glödtråd av trådrör), dussintals mindre element, till ett anodbatteri, vars spänning kunde nå 60-80 volt. Batterierna var "våta" - med flytande elektrolyt och krävde skötsel och underhåll.
sålunda, galvanisk cell, några ord "hur?" och "varför?" Elektrisk ström uppstår när metaller interagerar. I detta fall inträffar en annan potentialskillnad (spänning). Tillbaka 1793 etablerade Alessandro Volta, som konstruerade en galvanisk cell (Volta pol), den relativa aktiviteten för de då kända metallerna: Zn, Pb, Sn, Fe, Cu, Ag, Au. Galvaniccellens "styrka" visade sig vara större, desto längre var metallerna i denna rad (spänningsserien).

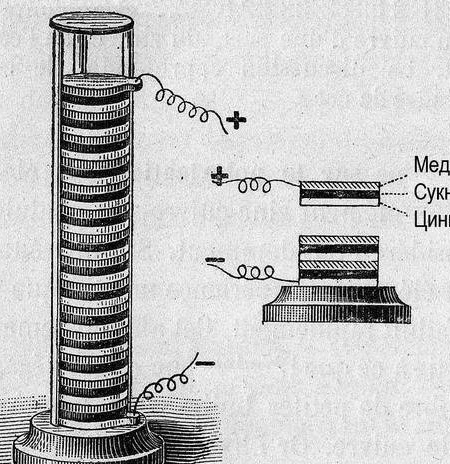
Senare, för att organisera data, togs potentialen för "väteelektroden" som en nollreferens. Efter att mäta potentialen hos metallerna i par med honom, arrangerades de experimentella metallerna i rad. Den resulterande tabellen kallades "Electrochemical Series of Metal Stresses" och måste i kemiskåpet hänga bredvid det periodiska systemet och porträttet av Dmitry Ivanovich.

Ett antal metallspänningar är en användbar kontrast, i vårt fall kommer vi, liksom Alessandro Volta, att veta - ju längre metallerna separeras från varandra, desto större kommer spänningen att erhållas.
I våra experiment, som klassikerna, använde vi koppar och zink.När plattorna är nedsänkta i elektrolyten mellan dem och zinkplattan inträffar en kemisk reaktion, som ett resultat av vilka negativa laddningar samlas på plattan och den är negativt laddad. Som ett resultat av reaktionen som äger rum i den galvaniska cellen upplöses zinkelektroden gradvis.
På en kopparelektrod, under drift av en galvanisk cell, bildas små vätebubblor som isolerar kopparnas yta från elektrolyten. Fenomenet kallas, i en galvanisk cell är det skadligt, de kämpar med det. För att avlägsna det frigjorda väte införs ämnen som kallas väte i elektrolyten. I deras roll är ofta föreningar av mangan, kopparsulfat. I enkla experiment kan kaliumpermanganat i apotek användas.
Vad vi använde för experimentet.
Enheter och material.
För montering av galvaniska celler, som kopparelektroder, kan du använda tråd, tråd, folie. Zink kan utvinnas från torra element, galvaniserade produkter kan användas. Istället för zink kan du försöka använda en elektrod av aluminium eller järn. Natriumklorid för elektrolyt, lite mjuk monteringstråd. Du behöver definitivt en voltmeter eller multimeter, trådknivar, saxar. Som kärl kan icke-metalliska behållare av lämplig storlek användas. Glas, bekvämare än lätta plastkoppar - de är tyngre, mer stabila, svårare att slå över. Det är mycket bra om det finns en lågströmslågspänningsbelastning - en enkel radio, en kvartsur etc.
"Högspänning" batteri av tråd och skruvar.
Fascinerad av enkelhetens detaljer och den relativt höga spänningen som mottogs försökte vi montera ett sådant batteri. Här används ett “klassiskt” metallpar - koppar-zink. Tanken är att använda galvaniserade fästelement som zinkelektrod. Lugnt. Det är uppenbart att ett sådant element inte är utformat för långsiktig drift - ett tunt lager av zink kommer snabbt att lösa upp, men detta är inte viktigt för ett kortvarigt experiment. Men galvaniserade skruvar eller kuggar är överallt fulla.
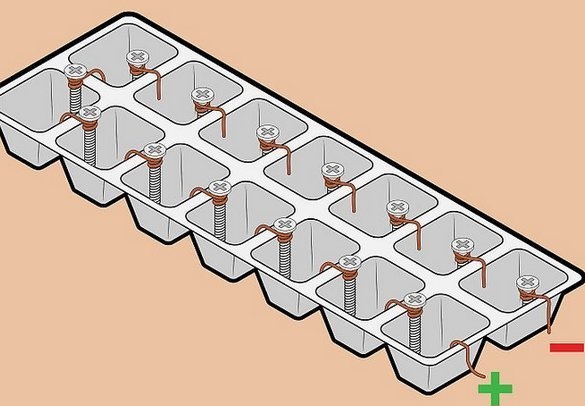
En tråd används också som en kopparelektrod - också ett allmänt tillgängligt material, dessutom - den mest praktiska installationen av element i ett batteri - alla element är anslutna i serie - plus ett till minus till nästa. I detta fall summeras spänningen, strömmen förblir densamma.
Låt oss komma igång.
Efter att ha valt önskat antal galvaniserade fästelement med önskad längd, hittade vi en lämplig koppartråd. Detta är en lindningstråd i lackisolering. Trådens diameter är cirka 0,5 mm.

Pole rengör lakisoleringen flera gånger med ansträngning för att dra i tråden genom en dubbelvecklad sliphud av medelstor storlek.


Sedan förbereder han ett par elektroder - under huvudet på en självspännande skruv, lindar tätt två eller tre varv tråd och skär bort överskottet.

Batteriaggregat - ett tåg användes som behållare för att frysa is. Du kan använda celler från boxade godis, men de är mer subtila. Efter att ha installerat elektroderna på väggarna mellan cellerna fyller vi behållarna med elektrolyt. Vi använde en lösning av bordsalt - en matsked med ett objektglas på 0,5 liter varmt vatten. För att fylla är det mycket bekvämt att använda en medicinsk spruta.


Vi hittade några fler skruvar för elektroderna och lägger till element i batteriet, det är vad vi fick. Spänningen vid en högimpedansbelastning (ingångsresistans för en digital voltmeter) är betydande, men vid varje belastning, dock märkbar, sjunker den avsevärt.
Försök att göra liknande galvanisk cell (batteri) med större elektroder.
Som behållare använde vi en halv liters burk (två), plattor med ett betydande område passar i den. Som elektroder tog vi tunn kopparfolie och zink - resterna av ett glas från ett fabriks "torrt" element, demonterades under framställningen av grafit för eldfast beläggning.

Vi rengörde resterna av torkade kristallina salter med en trådborste och klippte två plattor med ungefär sax med ungefär samma område. Skär två matchande ränder från kopparfolie. Också med sax. Vi fick två par elektroder, som utrustade våra element, utan vidare, böjde sina kanter på burkens hals.


I en större behållare beredde vi en elektrolyt - natriumklorid, löst i varmt vatten, koncentrationen är densamma och beredda element hälls.


Vi kopplade de två elementen i serie, med hjälp av en bit av fästtråden och två krokodilklämmor. Så bra, batterispänningen är nära standardfingret, försök att använda. Ett element med en spänning på 1,5 V används i en elektromekanisk klocka, dessutom är klockans strömförbrukning väldigt liten och vårt batteri kommer att kunna överdriva det.

Vi tog bort standardbatteriet från klockan och kopplade en bit av monteringsledningen till terminalerna. Genom att observera polariteten (kopparplatta - "+", zink - "-") anslöt vår klocka till ett provisoriskt batteri, voila! Klockan fungerar, spänningen "sjunker" till 1,3 V. Klockan fungerade perfekt i flera timmar, tills vi alla skröt (dock en trollkarl!) Då blev vi trötta.

Till banan.
Barns interna konstitution är sådan att uppmärksamhet på ett ämne, han kan fokusera inte mer än 15 ... 20 minuter, och alla klasser med barn bör planeras så att de passar in vid den tiden, eller växla mellan olika klasser, annars kommer du båda plågas.
Som en belastning är det bättre att tillämpa det, oavsett om det rör sig eller lysande - siffrorna på voltmetern imponerar sinnet, men inte hjärtat. Förutom klockor och miniräknare kommer det säkert att beundra arbetet från ett hemmagjordt batteri från en liten radiomottagare (som tillval - en hemgjord!).
För långvarig användning ska cellens elektrolyt skyddas mot damm och avdunstning och ta hand om depolariseraren - ja, åtminstone täppa till burken med en bit plastfilm med ett elastiskt band och tillsätt kaliumpermanganat till elektrolyten. Dessutom är det bättre att omedelbart samla det nämnda elementet i Popov.
Förutom galvaniserade självspännande skruvar är det möjligt att använda galvaniserat plåtstål, för stora element är det mer bekvämt - under experimentet kan du få en betydande ström och kraft oavsett (flytta fingrarna i luften).
Lista över begagnad litteratur.
1. P. Strelkov. Vet och kunna. Pioneer elektrotekniker. Detgiz. 1960 år
2. V.S. Polosin, V. G. Prokopenko. Workshop om metodik för undervisning i kemi. Moskva, "Upplysning", 1989, s. 202 203.

